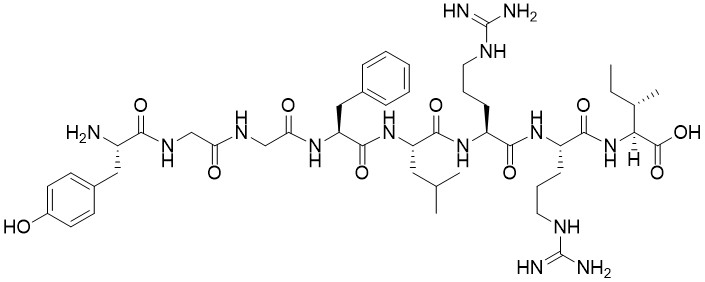
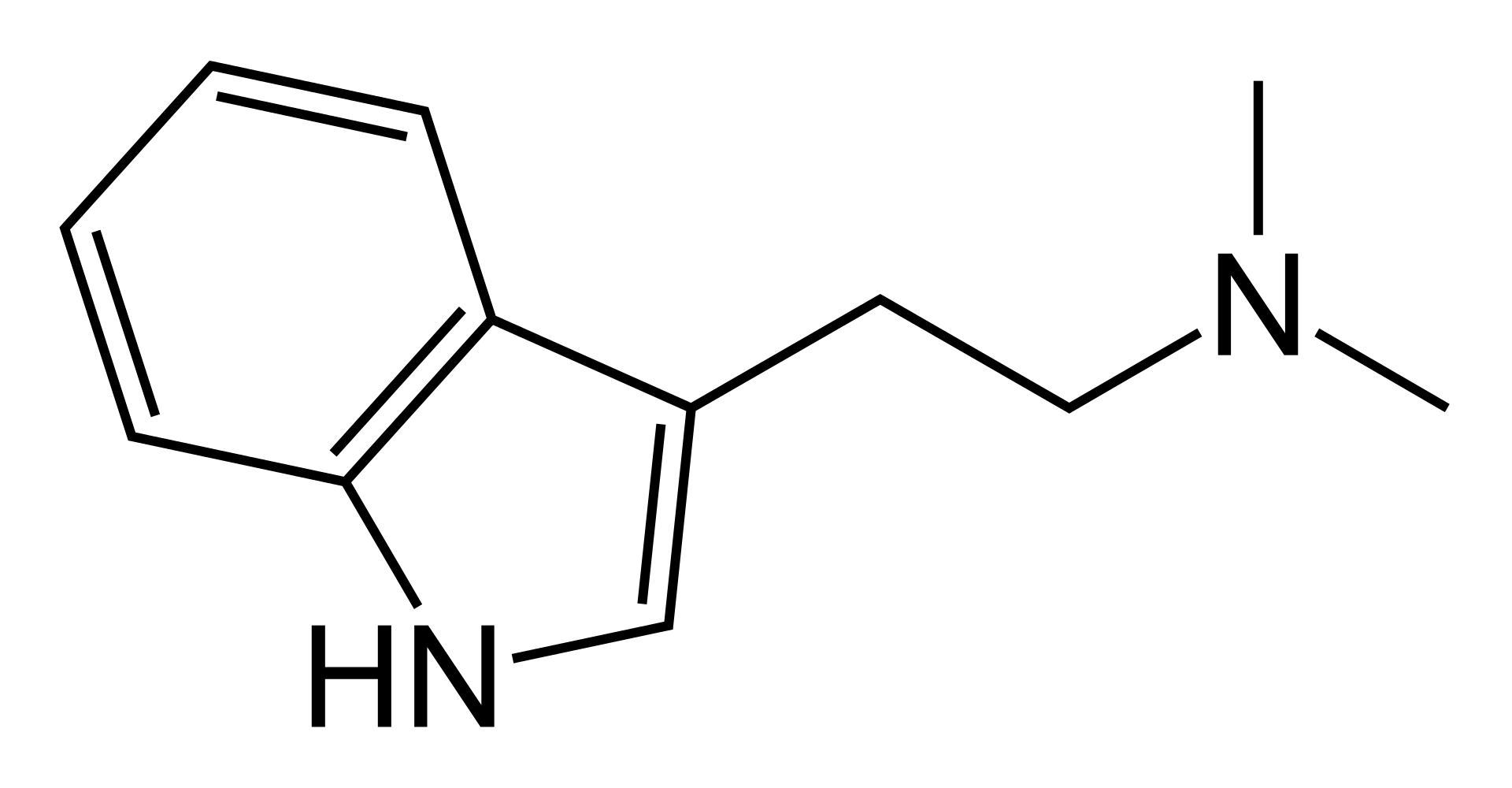
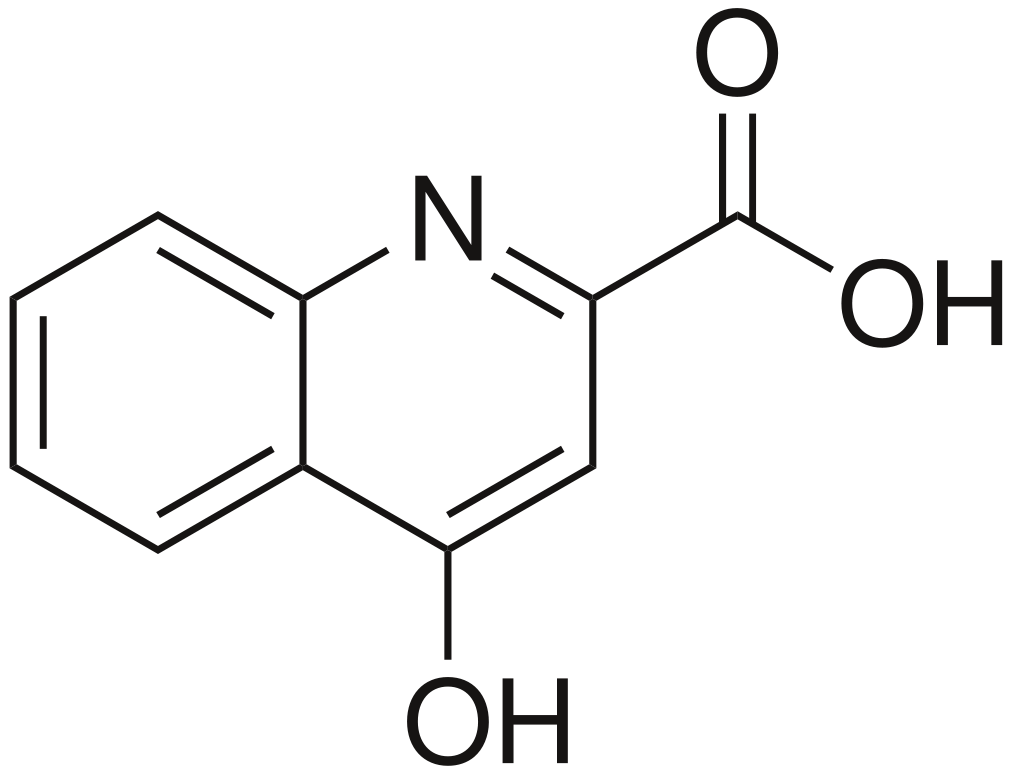
Динорфиновая гипотеза шизофрении
Оригинал за авторством theschizotypal
Люди, страдающие расстройствами шизофренического спектра, обычно переживают сильный психический стресс, приводящий к накоплению различных негативных переживаний. Имеются данные о том, что чрезмерные уровни стресса могут вызывать галлюцинации через механизм агонирования каппа-опиоидных рецепторов (KOR) и блокирования N-метил-D-аспаргиновых рецепторов (NMDAr). Предположительно, любой человек может выйти в психотический эпизод при достаточно продолжительном стрессе, а люди с шизофренией являются более восприимчивыми к последствиям стресса и менее способными их игнорировать, более того, могут существовать даже гены, обуславливающие стремление человека самостоятельно заводить себя в нонкомформистские, неприятные ситуации.
Здесь мы рассмотрим механизмы галлюцинаторных состояний, индуцированных стрессом. Динорфин, видимо, способен связать вместе многие имеющиеся гипотезы о нейрофизиологическом происхождении шизофрении. Динорфины - это семейство эндогенных опиоидов, которые преимущественно связываются с каппа-опиоидными рецепторами (KOR). Динорфин отвечает за вызванную стрессом дисфорию, ангедонию, тревогу, депрессивные и даже психотические состояния. Динорфин напрямую блокирует NMDA-рецепторы, что вызывает гипоактивность NMDA-комплекса, удовлетворяя глутаматной (кинуреновой) гипотезе шизофрении. Динорфин также снижает высвобождение глутамата. Считается, что хронически повышенный уровень дофамина играет роль в шизофрении; более того, он активирует динорфиновый комплекс - вероятно, за счет взаимодействия с D1- и NMDA-рецепторами. Динорфин усиливает активацию D2-рецепторов и снижает высвобождение дофамина, тем самым удовлетворяя дофаминовой гипотезе шизофрении.
— Динорфин и стресс. Динорфин участвует в механизмах, связанных с травматическими обстоятельствами, что объясняет связь шизофрении с сильным стрессом. Динорфин опосредует эффекты социального стресса и способствует социальной изоляции в раннем детстве, удовлетворяя теорию социального поражения шизофрении. Также было обнаружено, что социальная изоляция вызывает у животных изменения, подобные шизофрении. Связь социального отчуждения и шизофрении может свидетельствовать о том, насколько важна социальная поддержка для борьбы со стрессом. Тяжесть симптомов шизофрении коррелировала с отсутствием друзей. Было обнаружено, что частое общение с друзьями имеет огромное значение в терапии шизофрении, даже в большей степени, чем само качество дружбы. Социальные связи, даже в интернете, приносят пользу больным шизофренией. В экспериментальном исследовании было обнаружено, что одиночество увеличивает параноидную симптоматику, в то время как частое общение с людьми её снижает. Еще раз подчеркнем, что социальная изоляция в раннем возрасте усиливает влияние динорфинов в ЦНС. Картина социального поражения часто может начинаться с интереса к не распространённым в обществе вещам, который возникает до появления каких-либо психотических симптомов у шизофреников. Обретение странной веры, такой как теория плоской Земли, может подвергнуть человеку остракизму из-за клейма “сомнительных” убеждений. Затем, когда человек начинает подвергаться стигме и социальной изоляции, симптомы только продолжают ухудшаться. Общение может быть ключом к избавлению от стресса. Те, у кого нет социальной поддержки, могут быть не в состоянии даже оправиться от переживаний. Похоже, именно так обстоит дело с одиночным заключением, которое вызывает у заключенных множество шизофреноподобных симптомов, включая галлюцинации, сверхценные идеи, бред преследования и многое другое. Вероятно, психотические эффекты могут проявиться у любого человека, который находится в крайне отталкивающих и отчуждённых обстоятельствах, однако люди, рожденные с некоторым набором генов, связанных с шизофренией, являются более чувствительными к подобным травматическим ситуациям. Это также подтверждается корреляцией между низким социально-экономическим статусом и шизофренией: лица с низким социально-экономическим статусом с большей вероятностью испытают более тяжелые условия жизни, стресс и отчуждённость.
— Когнитивный дефицит. Люди с шизофренией часто страдают от когнитивного дефицита. В ходе исследования обнаружилось обширное совпадение локусов генов, связанных с плохой когнитивной способностью и шизофренией. Низкий IQ также коррелирует с шизофренией, и динорфин может помочь объяснить это. Микроинъекции динорфина в гиппокамп крыс вызывали дефицит пространственной памяти - люди с шизофренией также сталкиваются с дефицитом пространственной памяти. Было обнаружено, что динорфин повышается при возрастном снижении когнитивных функций, при том удаление генов, связанных с динорфином, ослабляет нейродегенеративные процессы, что было изучено при болезни Альцгеймера. Связанные с алкоголем нарушения памяти и обучения опосредованы активацией динорфина. Вызванный стрессом дефицит обучения и памяти опосредован динорфином. Динорфин играет роль в посттравматическом стрессовом расстройстве, что также связано с низким IQ. Другое геномное ассоциативное исследование обнаружило убедительные доказательства генетического совпадения между посттравматическим стрессовым расстройством и шизофренией. Это подтверждает идею о том, что люди с шизофренией рождаются с более высокой чувствительностью к стрессу. Вдобавок ко всему, социальная изоляция резко снижает IQ (25%) и способность к рассуждению (30%) в краткосрочной перспективе. Это важно, поскольку стресс от социального поражения опосредуется динорфином.
— Динорфин и психозы. Динорфин и его роль в психозах до сих пор не исследованы в полной мере. Агонисты каппа-опиоидных рецепторов (KOR), такие как динорфины, вызывают психотические состояния у здоровых людей. Считается, что динорфины высвобождаются во время судорог, чтобы компенсировать гиперактивность глутамата, но они также способны вызвать психоз после приступа. Рецепторные комплексы дофамина D1 и D2 локализуются на динорфиновых нейронах у пациентов с шизофренией, что является важным из-за влияния рецептора D1 на повышенную активность динорфинов. Было обнаружено, что уровни динорфинов увеличены в спинномозговой жидкости шизофреников и коррелируют с тяжестью их психотических симптомов. Стимуляторы, такие как кокаин, амфетамин и никотин повышают влияние динорфинов, что может объяснить индуцируемый ими стимуляторный психоз. Существует явление, известное как «кокаиновые жуки», то есть ощущение ползающих насекомых: эффект, который инъекции динорфина вызывают у каждого четвёртого наблюдаемого субъекта. Также было показано, что антагонисты динорфиновых рецепторов действуют как антипсихотические средства быстрого действия. Напротив, агонисты KOR способны индуцировать психотические состояния: “Вдыхание испаренного сальвинорина-А привело к очень сильным психотропным эффектам с быстрым началом и малой продолжительностью. Изменённое восприятие включало зрительную область, и, в отличие от агонистов 5HT2A-рецепторов, были сильно распространены слуховые галлюцинации. Также, в отличие от классических серотонинергических психоделиков, потеря контакта с внешней реальностью была заметной, поскольку участники не реагировали на внешние визуальные и вербальные сигналы, особенно после средних и высоких доз. В то время как при низких и средних дозировках наблюдалось усиление телесных ощущений, при приеме 1,0 мг наблюдалась почти полная потеря обладания телом и увеличение внетелесных ощущений. Эти результаты предполагают, что система динорфинов - KOR может играть ранее недооцененную роль в регуляции сенсорного восприятия, интероцепции и чувства владения телом у людей.” Это исследование великолепно, потому что оно отличает динорфиноподобные психотические эффекты, такие как “голоса в голове”, от серотонинергических психоделических состояний, которые довольно редко содержат слуховые голосовые галлюцинации. Напомним, динорфин является агонистом KOR, аналогичным препарату Salvia Divinorum (Шалфей Предсказателей). По сути, это и есть эндогенная сальвия. Это означает, что социальное отторжение и даже стресс в целом могут вызывать галлюцинаторные и психотические эффекты, подобные сальвии. Люди, имеющие гены, связанные с шизофренией, вероятно, обладают естественной чувствительностью к стрессу, сниженной способностью восстанавливаться после него, более высокой вероятностью вести неблагоприятный для здоровья и общества образ жизни.
— Нейрогенез и нейропластичность. Нейрогенез - это процесс рождения новых нейронов. Нейропластичность - это способность реорганизовывать синаптические связи, в частности в ответ на обучение. У больных шизофренией нарушен нейрогенез и нейропластичность. Нейрогенез усиливается за счет долгосрочной потенциации (LTP), которая зависит от активности NMDA-рецепторов. Есть свидетельства того, что у шизофреников нарушена LTP, вероятно, за счёт гипофункции NMDA-комплекса. Считается, что эта гипофункция NMDAr, наблюдаемая при шизофрении, может объяснить снижение нейрогенеза. NMDA-рецепторы также играют решающую роль в нейропластичности, поэтому гипофункция этих рецепторов также может объяснить её снижение, наблюдаемое при шизофрении. Было обнаружено, что стресс снижает интенсивность нейрогенеза. Антагонисты каппа-опиоидных рецепторов (KOR) могут действовать как антипсихотические препараты. Динорфин снижает LTP и снижает возбуждающую передачу сигналов в гиппокампе, а также в зубчатой извилине, по крайней мере, частично объясняя уменьшение объема гиппокампа, связанное со стрессом. Хроническое употребление опиатов усиливает активность динорфина и подавляет нейрогенез. Неясно, подавляет ли динорфин сам нейрогенез, но это кажется вероятным благодаря вышеуказанным исследованиям. В некоторых исследованиях упоминается гипотеза о том, что динорфин увеличивает нейропластичность. Считается, что повышение нейропластичности может иметь потенциал в лечении шизофрении. Теанин является частичным агонистом NMDAr, который, как было установлено, действует как слабое антипсихотическое средство, а также усиливает нейрогенез.
— Глицин. NMDA-рецептор имеет подсайт глицина, который является необходимым кофактором для стимуляции рецептора. Глутамат может активировать NMDA-рецептор, если глицин занимает субсайтовый рецептор. Динорфин способен связываться не только с основным сайтом NMDA-рецептора как антагонист, но также, по-видимому, и с глициновым субсайтом. Обычно связывание на субсайте глицина позволяет глутамату активировать NMDA-рецептор. Когда внеклеточные уровни глицина низкие, динорфин заменяет функцию глицина, усиливая активность NMDAr. Предполагается, что динорфин блокирует N-метил-D-аспаргиновый рецептор, когда участки глицина заняты либо им самим, либо динорфином. При низком уровне глицина большая часть динорфинов может замещать функцию глицина. Возможно, очень высокие уровни динорфина приводят к заселению динорфином как субсайта глицина, так и основного сайта NMDA-рецептора, тогда как при высоких уровнях глицина динорфин занимает в основном сайт NMDAr. Если уровни глицина низкие, динорфин, вероятно, действует как усилитель и антагонист NMDAr, но преобладать будет именно активация N-метил-D-аспаргинового рецептора. Динорфин может по-разному вызывать диссоциативный или обезболивающий эффект в зависимости от внеклеточного уровня глицина. Если активность NMDAr усиливается, следует ожидать усиления болевого и эксайтотоксического действия. Возможно, шизофреники испытывают и то, и другое в зависимости от их метаболизма глицина в ЦНС.
— Серотонин и глутамат. Психоделики действительно могут иметь огромное значение в терапии заболеваний шизофренического спектра, хотя это противоречит интуиции многих людей. Психоделики - это агонисты серотонинергических 5-HT2A рецепторов. Здесь мы обсудим ЛСД, псилоцибин, ДМТ и МДМА. Психоделические препараты усиливают нейрогенез в гиппокампе, области головного мозга, объем которой уменьшается у людей с шизофренией. Серотонин также может индуцировать нейрогенез. Психоделики способствуют структурной и функциональной нейропластичности, которая, как упоминалось ранее, нарушается при шизофрении. Было обнаружено, что ЛСД ослабляет депрессивные эффекты агонизма каппа-опиоидных рецепторов. С другой стороны, было обнаружено, что обратные агонисты 5-HT2Ar усиливают динорфиновую передачу сигналов. Психоделики также недавно стали рассматриваться как средство лечения посттравматического стрессового расстройства. Механизм действия ЛСД, направленный "против" динорфина, связан с 5-HT2A и 5-HT1A рецепторами. Рецепторы 5-HT1A подавляют высвобождение динорфина, которое происходит при применении различных дофаминергических препаратов. Рецепторы 5-HT2A увеличивают высвобождение ацетилхолина в гиппокампе и префронтальной коре, что важно, поскольку один из холинергических рецепторов, nAChRα7, подавляет высвобождение динорфина. Считается, что при шизофрении рецептор nAChRα7 не способен работать в полной мере; данное предположение привело к экспериментальному лечению с использованием агонистов nAChRα7-рецептора. Рецептор 5-HT2A также подавляет активность mGlur2, метаботропного рецептора глутамата, который в норме может способствовать активности динорфина. И 5-HT1A-, и 5-HT2A-рецепторные комплексы связаны с подавлением отвращения, что хорошо согласуется с данной гипотезой, поскольку динорфин участвует в формировании отвращения, и это действие серотонина, по-видимому, подавляет динорфин.
Динорфин участвует в развитии депрессии. Между тем, однократное употребление большой дозы псилоцибина вызвала длительное (6+ месяцев) уменьшение депрессивной симптоматики у 80% пациентов, умиравших от неизлечимой болезни. В другом исследовании псилоцибина при депрессии все пациенты показали положительный эффект через 1 неделю после приема дозы, а многие из них сохранили положительный эффект в течение множества недель. Сканирование с помощью фМРТ показало, что снижение притока крови к миндалине, вызванное псилоцибином, коррелирует со снижением депрессивных симптомов, в то время как динорфин связан с усилением тревожности у человека. В метаанализе 2020 года изучалось исследование псилоцибина для лечения тревожности и депрессии, и также было обнаружено снижение их интенсивности. Кроме того, динорфин играет важную роль в развитии зависимости, а псилоцибин смог избавить 80% курильщиков от никотина при употреблении только разовой дозы. Исследование 2016 года показало, что псилоцибин даже уменьшает негативные ощущения, вызываемые социальной изоляцией, которые имеет огромную связь с динорфином, социальным отторжением и шизофренией. Все это приводит к мысли, что психоделики могут обращать действие динорфина и снижать интенсивность индуцированных им эффектов.
Динорфин и психоделики связаны с явлением страха. При шизофрении механизм его угасания нарушен. Было обнаружено, что блокирование каппа-опиоидных рецепторов блокирует и условный страх. Более того, низкие дозировки ДМТ, псилоцибина и МДМА приводят к такому же результату. Во время исследований по распознаванию страха, которые измеряют реакцию миндалины, люди, страдающие шизофренией, демонстрируют гиперактивацию миндалевидного тела как на испуганные, так и даже на нейтральные лица, в то время как у исследуемых, принимающих ЛСД, реакция миндалины снижается. Эта изменённая реакция на страх возвращает нас к идее о том, что люди с шизофренией могут быть менее способными оправиться от стрессовых событий, что приводит к накоплению негативных эмоций. Похоже, что серотонин и динорфин выполняют противоположные и взаимосвязанные роли в эмоциональной устойчивости и стрессе. Блокирование динорфина напрямую приводит к стрессоустойчивости. Известно, что сам серотонин подавляет активность SERT, белка, осуществляющего его обратный захват. Это означает, что увеличение активности серотонина должно снижать регуляцию SERT и снижать способность динорфина оказывать свои эффекты. Точно так же, когда уровни динорфина высоки, его индукция SERT снижает уровни внеклеточного серотонина и предотвращает подавление SERT. Было обнаружено, что повторные дозы агониста каппа-опиоидных рецепторов, Шалфея Предсказателей (Salvia Divinorum), также повышают регуляцию SERT, что наблюдается и при шизофрении. Более того, стресс социального отторжения на животных моделях тоже активизирует SERT. В конечном счете, картина низкой активности серотонина и высокой активности динорфина согласуется. Возможно, что нарушение KOR-опосредованных эффектов, вызванных психоделиками, останавливает эту петлю, в которой индуцируется SERT, тем самым позволяя серотонину снова накапливаться и восстанавливать устойчивое состояние ума. Было обнаружено, что у людей с шизофренией менее функциональные рецепторы 5-HT2A. Ген, связанный с меньшим количеством рецепторов 5-HT2A, был связан с шизофренией, и впоследствии пациенты с шизофренией имели более низкое содержание мРНК рецептора 5-HT2A в гиппокампе и префронтальной коре. Представляется весьма вероятным, что люди с эндогенными психоделическими состояниями, схожими с HPPD (длительное расстройство восприятия, вызванное употреблением галлюциногенов) будут считаться шизофрениками наряду с теми, кто испытывает более классические симптомы шизофрении, такие как “голоса в голове”. Это значительная проблема, но давайте продолжим.
Рецептор 5-HT2A образует комплексы с метаботропным глутаматным рецептором mGlur2, который считается необходимым звеном для психоделических эффектов. Исследование показало снижение функции этих “психоделических рецепторных комплексов” в головном мозге людей, страдающих шизофренией. Поскольку агонизм mGlur2 усиливает связывание 5-HT2A-рецептора, сниженную активность 5-HT2A можно объяснить сниженным количеством mGlur2, которое и наблюдается в исследовании. Стоит отметить, что это исследование показало увеличение числа 5-HT2A-рецепторов у шизофреников. Более низкая плотность рецепторов mGlur2 может означать, что у шизофреников более низкая способность активировать 5-HT2A-комплекс и, как следствие, психоделический механизм. Агонизм рецептора 5-HT2A требовал присутствия рецептора mGlur2 для проявления его эффектов у животных, поэтому, хотя эффект рецептора 5-HT2A заключается в снижении активности mGlur2, отсутствие mGlur2 предотвращает возникновение каких-либо эффектов. В более ранних исследованиях это подтверждается. Шизофреники, по-видимому, менее чувствительны к ЛСД, а также демонстрировали снижение эффектов от ДМТ, испытывая недостаток визуальных эффектов при дозах, которые работали у нешизофреников. Препараты глицинового ряда, которые могут лечить шизофрению за счет усиления NMDAr, увеличивают серотонин в префронтальной коре головного мозга, где находятся рецепторы 5-HT2A. Другое исследование показало, что низкая таламокортикальная пластичность модулируется дисфункциональными рецепторами 5-HT2A при шизофрении. Напомним, что серотонин, препараты глицинового ряда и психоделики индуцируют механизм нейропластичности. Главный симптом шизофрении - когнитивный дефицит. У людей с шизофренией также наблюдается нарушение ассоциативного обучения. Было обнаружено, что психоделики улучшают когнитивные функции и увеличивают способность к ассоциативному обучению. Антагонисты рецептора 5-HT2A были способны снижать речевую и пространственную память у лиц, предварительно получавших СИОЗС. В совокупности это может означать, что более низкое функционирование рецепторов 5-HT2A может позволить неослабленной активности динорфина нарушать когнитивные функции при шизофрении, аналогично тому, как это наблюдается при когнитивном дефиците, связанном со стрессом. Поскольку психоделики ослабляют эффекты динорфина, возможно, ослабляются и когнитивные нарушения, связанные с его действием. Другое исследование показало, что потеря mGlur2 коррелирует с возрастом, а не с диагнозом шизофрении. Связывание с рецептором 5-HT2A также ослабляется с возрастом. Ослабление связывания 5-HT2A-рецепторов связано с когнитивными нарушениями. Кроме того, когда гены, продуцирующие динорфин, удаляются из мышей, возрастная потеря mGlur1 уменьшалась вместе с возрастным снижением когнитивных способностей. Каким-то образом активность динорфина приводит к потере mGlur1 при старении, поэтому, возможно, динорфин может быть причастен к потере mGlur2, которая также наблюдается при старении. Потеря mGlur2 с возрастом будет означать, что связывание 5-HT2A уменьшается, что приводит к усилению действие динорфина, что, по-видимому, является порочным кругом. Это может служить моделью когнитивного старения как динамики между серотонином, динорфином и глутаматом. В случае шизофрении это может частично объяснить "ускоренное старение".
Многие исследования посвящены идее, что психоделики являются аксиоматической моделью шизофрении. Недавние исследования шизофрении, в которых использовался агонист mGlur2, потерпели неудачу на третьей фазе. Этот препарат работал как агонист mGlur2, активно влияющий на 5-HT2A-рецепторы. Связывание с 5-HT2A-рецепторами снижает активность mGlur2, что позволяет увеличить высвобождение глутамата, которое обычно ингибируется mGlur2. Этот экспериментальный препарат действовал на рецептор mGlur2 в противоположном направлении, нежели психоделики, усиливая рецептор, а не снижая его активность. Было обнаружено, что этот препарат корректирует некоторые опосредованные антагонистами NMDAr нарушения гамма-ритма, но не восстанавливает опосредованные антагонистами NMDAr проблемы с когнитивными функциями. Было обнаружено, что агонисты mGlur2 предотвращают нейротоксичность, вызванную антагонистами NMDA-рецепторов, но есть доказательства того, что психоделики также делают это. Прием препарата мог не сработать из-за потенциальных эффектов усиления динорфина. Поскольку агонизм mGlur2 снижает высвобождение глутамата, он противодействует усилению глутамата антагонистами NMDAr. Возможно, что препарат помогает при определенных симптомах, усиливая передачу сигналов 5-HT2A, но также и препятствует другим механизмам передачи сигналов, действуя противоположным образом.
Толерантность и уменьшение числа рецепторов могут быть проблемой. Психоделики с коротким действием, такие как ДМТ, гипотетически могут вызывать меньшую толерантность, поэтому они предпочтительнее, чем психоделики длительного действия, такие как ЛСД. Было замечено, что более поздняя фаза интоксикации ЛСД стала более параноидной и, казалось бы, психотической, что привело к исследованиям, показывающим, что хроническое употребление ЛСД приводит к психотическим нарушениям. В этом исследовании они упомянули изменения в экспрессии генов в качестве объяснения. Альтернативным объяснением может быть уменьшение связывания 5-HT2A. Было обнаружено, что хроническое введение ЛСД снижает связывание 5-HT2A в головном мозге и вызывает толерантность к эффектам, что и характерно для шизофреников, как снижение связывания лиганд с рецепторами, так и меньшая чувствительность к психоделическим эффектам. Было обнаружено, что как разовый, так и хронический прием ЛСД вызывает повышение уровня серотонина. Эта повышенная активность может быть способна подавлять переносчик серотонина, SERT, тем самым снижая способность динорфина оказывать своё действие и обеспечивая тенденцию к повышению уровня серотонина в ЦНС. В некотором смысле, это может обратить вспять чувствительность к стрессу и повысить склонность к "сопротивлению" психотической симптоматике. Хроническое употребление психоделиков может вызвать состояние, подобное абстиненции, что приведет к усилению передачи сигналов динорфина, что может лишь усугубить проблемы. Редкое употребление ДМТ может помочь избежать некоторых из этих проблем из-за непродолжительности его действия. Частое употребление может вызвать долговременные проблемы, сходные с шизофреноподобными состояниями, подобно тому, как длительное использование бензодиазепинов вызывает беспокойство и судорожные расстройства при резком прекращении их применения. Можно сделать вывод, что психоделики могут способствовать терапии шизофрении, нарушая психотомиметические сигналы каппа-опиоидной системы. Неясно, потребуется ли частое их использование или, как в случае депрессии, однократная доза может дать длительные эффекты. Я подозреваю, что это зависит от образа жизни пациента, поскольку психоделические препараты могут помочь именно в устойчивости и адаптации к стрессу.
— Кинуреновая кислота (KYNA). В последние годы появилась новая гипотеза о нейрофизиологическом происхождении шизофрении после того, как было обнаружено, что у пациентов, больных шизофренией, повышен уровень кинуреновой кислоты в их спинномозговой жидкости. Как и динорфин, стресс вызывает выброс кинуреновой кислоты. Кинуреновая кислота (KYNA) представляет собой метаболит L-триптофана, являющийся неселективным антагонистом глутаматных рецепторов и глицинового субсайта. Кинуреновая кислота, блокируя субсайт глицина, не даёт глутамату связываться с NMDA-рецептором, из-за чего глицин не используется, накапливаясь во внеклеточной среде. Именно поэтому динорфин с большей вероятностью действует непосредственно на NMDA-рецептор как антагонист, а не как заменитель глицина на субсайте. Таким образом, кинуреновая кислота самостоятельно вызывает эндогенные диссоциативные состояния, которые также складываются с диссоциативными галлюциногенными эффектами динорфина и многократно усиливаются.
Более того, существует странная связь между ниацином и шизофренией; ниацин является важным ферментом в метаболизме L-триптофана. В некоторых случаях ниацин оказался эффективным средством в терапии шизофрении. Психоз также является признаком дефицита ниацина. Исследование показало, что недостаток ниацина является признаком шизофрении. В более позднем исследовании 2016 года было отмечено, что ослабленный ответ на ниацин зависел от тяжести течения шизофрении, поскольку пациенты с ультравысоким риском психоза имели преувеличенную реакцию в виде приливов крови. Бредовый паразитоз и ощущение ползания мурашек, связанные с пеллагрой, в прошлом эффективно и быстро лечились ниацином. Прилив крови, индуцированный ниацином, вызывает высвобождение серотонина из тромбоцитов и блокируется на 85% с помощью специфического антагониста 5-HT2A-рецепторов. В другом исследовании изучались приливы и высказывались предположения, что рецепторы 5-HT2A, по-видимому, играют ключевую роль в их возникновении. В связи с тем, что у людей, больных шизофренией, наблюдаются проблемы с комплексом 5-HT2A-рецепторов, это может объяснить сниженный приток крови от ниацина. Поскольку L-триптофан является предшественником синтеза серотонина, гиперпродукция KYNA может быть результатом неспособности синтезировать серотонин или того, что синтез серотонина отключен из-за частого обратного захвата, индуцированного динорфином. Почему может увеличиваться синтез KYNA? L-триптофан метаболизируется двумя путями: либо к серотонину и мелатонину, либо к KYNA. Токсоплазмоз связан с шизофренией, и было обнаружено, что он сопровождается секрецией фермента, который приводит к деградации триптофана в направлении пути KYNA и в сторону от пути серотонина, что приводит к снижению уровня серотонина и увеличению KYNA.